具翻译功能的 Circ-ZNF609及其在肌生成中的功能研究
Circ-ZNF609 Is a Circular RNA that Can Be Translated and Functions in Myogenesis
circRNA以独特的结构参与转录,但其功能仍有待研究。目前circRNA通过反剪接反应的生物合成方式已被广泛认同,然而他们在生理相关过程的调节作用仍未阐明。本文研究circRNA在小鼠和人类成肌细胞的体外分化过程中的表达差异,发现高保守circRNA的表达水平受肌生成和杜氏营养及不良症(DMD)状态的影响。采用高通量功能基因筛选来研究肌分化中circRNA的功能,发现Circ-ZNF609能特异性地调节成肌细胞的增殖。令人意外的是,与线性转录子一样,Circ-ZNF609包含了一个从起始位点到终止位点的开放阅读框架(ORF)。除此,Circ-ZNF609能与高密度多核糖体结合,且能以剪切依赖和帽子不依赖的方式翻译蛋白。这为真核细胞circRNA能编码蛋白提供了一个有利的证据。
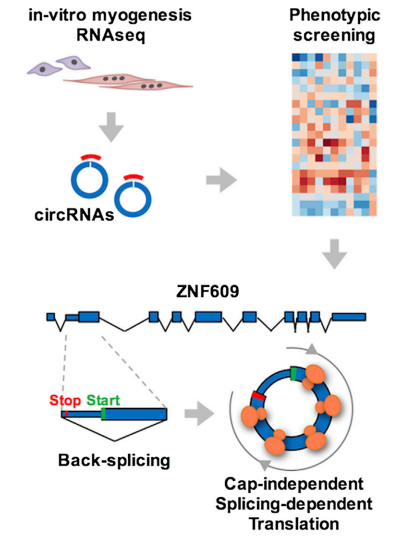
环状RNA是一种非编码RNA,其通过反剪接产生,以共价键形成闭合环,不具有5’帽子和3’尾巴结构。它可以作为miRNA海绵调控靶基因的表达,也可以与多种蛋白结合发挥不同的生物学功能。尽管环状RNA已在多种细胞组织中被研究,但其对生物代谢过程的调控作用仍有待研究。
目的
研究肌生成相关的circRNA及其在肌生成和肌肉疾病中的作用。
1、肌细胞内circRNA表达丰富,进化高保守
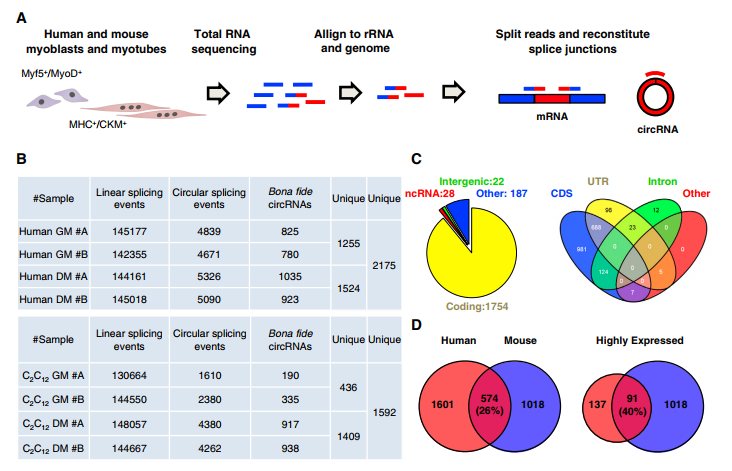
通过RNA-Seq筛选人源和小鼠(C2C12)成肌细胞(GM, myoblasts)分化为肌管细胞(DM, myotubes)过程以及杜氏肌营养不良症状态下差异表达的circRNA,并采用FindCirc软件检测circRNA(图1A)。检测到人和小鼠的GM和DM中均存在丰富的circRNA(图1B)。对这些circRNA进行基因组区域(GO)注释,发现近90%的circRNA源自编码蛋白基因的外显子区(图1C)。此外,研究人员发现有相当一部分的circRNA(特别是高表达的circRNA)在人类和小鼠之间具有较高的保守性(图1B, 1D)。
2、肌肉分化和疾病对circRNA表达的影响
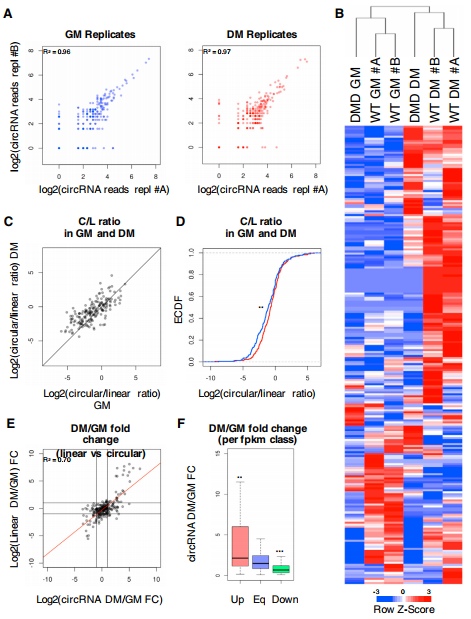
本文研究circRNA表达差异,仅将来源于人类样本、至少含有5个反剪接反应(back-splicing) reads的circRNA纳入研究。图2A表明GM和DM各自的两个重复样本间的circRNA具有非常好的相关性,说明两个重复之间具有高度的一致性。从整体上观察肌肉分化及疾病状态下circRNA表达谱差异(图2B),结果展现了两种差异:第一,人源GM和DM之间circRNA的表达存在较大差异,说明肌分化能调节circRNA的表达;第二,相比正常人,肌营养不良症病人的GM与DM中均存在着大量异常表达的circRNA,说明疾病状态也影响circRNA的表达(图2B)。circRNA与linear RNA比率的结果已与上述结果一致(图2C,2D)。进一步探究差异表达的circRNA与linear RNA的关系,发现circRNA和linear RNA之间的表达呈现正相关关系(图2E)。此外,circRNA的丰度显著高于无差异和下调组,即上调基因的差异比较显著(图2F)。
3、 基于RNA干扰技术的circRNA功能筛选
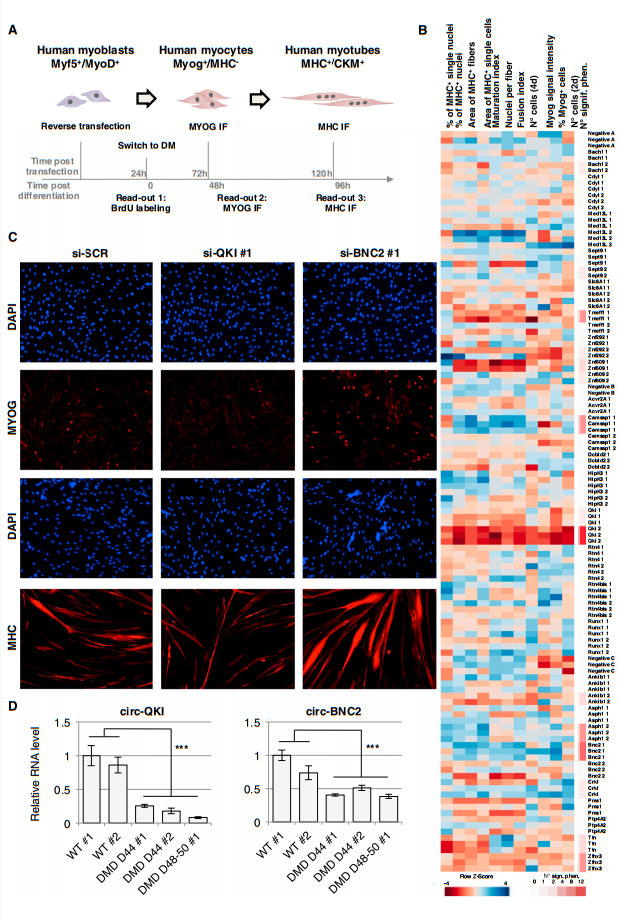
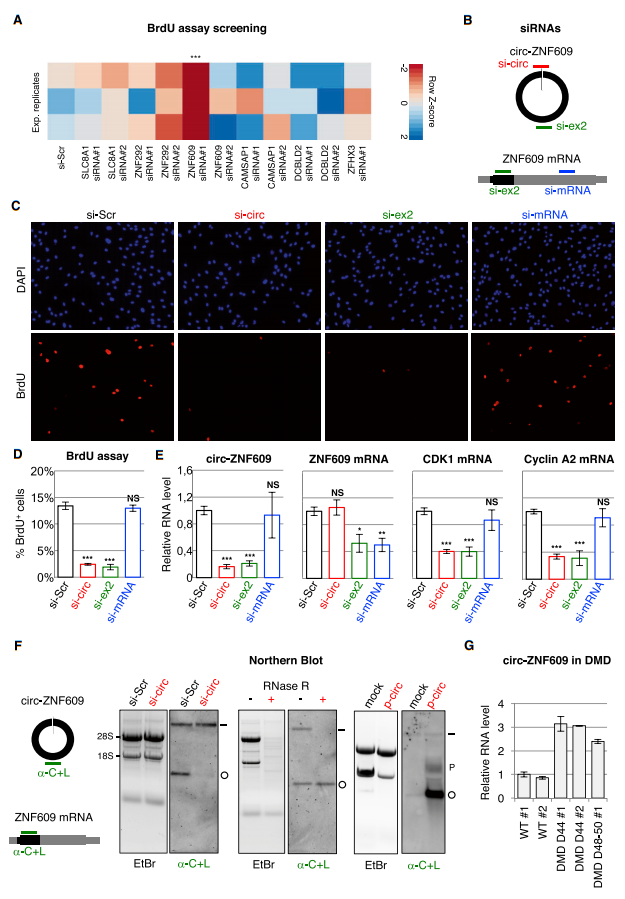
根据circRNA的保守性、表达丰度、调控分化作用和环化率4个指标,研究在肌分化过程中具有重要作用的circRNA,筛选到31个候选circRNAs。在RT-PCR和RNase R抗性实验确证后,研究人员对20个circRNAs进行了45个siRNAs干扰。进一步的溴脱氧尿苷(BrdU)标记实验(图4A)显示,敲低circ-ZNF609明显抑制了细胞的增殖(约80%),提示其在成肌细胞增殖过程中可能起着重要调控作用。随后发现敲低circ-ZNF609亦能抑制增殖标志物CDK1和cyclin A2的蛋白表达(图4E)。此外,在DMD病人的成肌细胞中circ-ZNF609的表达明显升高(图4G)。以上结果表明,circ-ZNF609可通过调控细胞增殖影响肌生成。
4、Circ-ZNF609能编码蛋白
深入研究后发现,Circ-ZNF609是由ZNF609基因的第二个外显子开始环化形成。令人意想不到的是,Circ-ZNF609竟含有一个753-nt的开放阅读框(ORF),其中包含转录起始位点和终止密码子(图5A)。另外,通过蔗糖梯度分离实验发现Circ-ZNF609与高密度的多核糖体存在结合(图5B),这意味着circ-ZNF609可能编码蛋白质。为确证circ-ZNF609是否具有编码蛋白质的能力,研究人员对能特异性过表达Circ-ZNF609的p-circ载体进行结构改造,利用CRISPR/Cas9技术在p-circ基础上添加3×Flag标签,构建了p-circ 3xF载体(图6A)。利用过表达和突变实验,验证了Circ-ZNF609的结构中关键位点(两个起始位点)对于编码蛋白的作用。此外,热应激(2h 44℃)能使circ-ZNF609的翻译能力增强(图6F)。以上实验表明,CircZNF609能翻译蛋白,且该过程受热应激诱导。

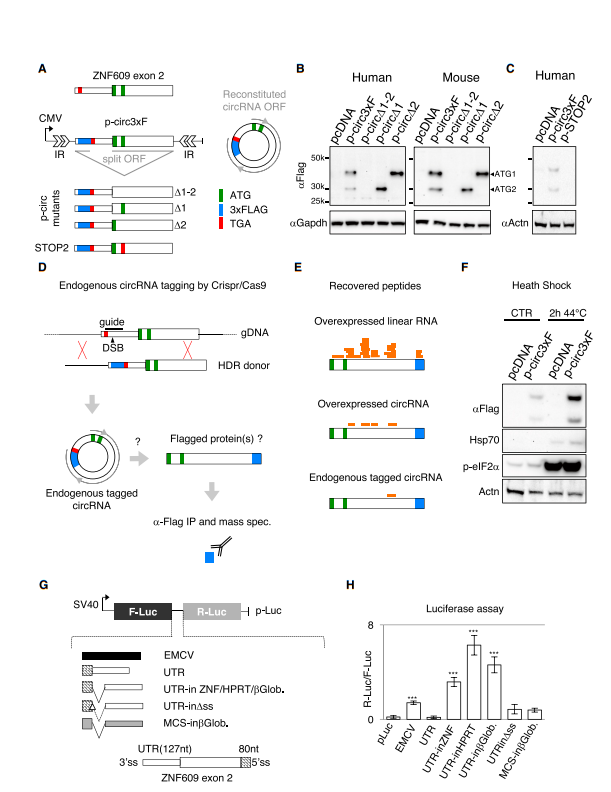
5、IRES激活Circ-ZNF609的UTR(非编码区)
由于circRNA没有帽子结构(cap),其翻译需要一个IRES序列(内部核糖体进入位点)。为检测Circ-ZNF609是否具有IRES活性,研究人员将其UTR插入双顺反子结构的萤火虫和海肾萤光素酶之间,构建荧光报告酶基因(6G)。结果显示,内源性Circ-ZNF609的UTR具有依赖于剪接方式的IRES活性(6H),即Circ-ZNF609能在IRES的驱动下以剪切依赖的方式翻译蛋白质。
经验总结
该研究的初始目的是寻找肌生成特异相关的circRNA,通过前期的高通量筛选、利用siRNA技术进行的功能性筛选发现了具有翻译功能的Circ-ZNF609,后期实验则是对其翻译功能的验证和机制探索。该研究不仅找到多种与肌生成特异相关的circRNAs,更重要的是发现了能够翻译蛋白质的Circ-ZNF609。我们从中得到启示:大的发现往往是在不经意时被挖掘的,但其前提是要不懈努力、不断地研究探索。
Legnini I, Timoteo G D, Rossi F, et al. Circ-ZNF609 Is a Circular RNA that Can Be Translated and Functions in Myogenesis[J]. Molecular Cell, 2017, 66(1):22.
文:永诺生物





来第一个抢占沙发评论吧!