原创作者:联创生物|微信公众号
circRNA是目前十分热门的研究方向,有研究表明circRNA呈发育调控、组织/细胞特异表达,其参与了各种复杂的调控过程,但关于circRNA在牛成肌细胞的分化过程中的作用还未见报道。随着高通量测序技术的发展和进步,大量的circRNA在不同物种中被鉴定。
联川客户西北农林科技大学的研究者们通过一次测序实验,后续从不同角度对测序数据进行挖掘,发表了4篇高质量的ceRNA文章。研究方向包括成肌细胞增殖、分化和存活的调控等,文章围绕ceRNA的几类核心分子——circRNA,miRNA,lncRNA进行了深入的分析。该课题的研究方法及撰文思路十分新颖,可为广大科研工作者提供一些新思考。
文章信息
circFGFR4 Promotes Differentiation of Myoblasts via Binding miR-107 to Relieve Its Inhibition of Wnt3a
发表单位:西北农林科技大学
发表期刊:Molecular Therapy
影响因子:7.008
发表年份:2018
研究内容:circRNA调控成肌细胞分化以减轻Wnt3a的抑制作用

研究背景
随着第二代测序技术的发展,过去数十年功能性非编码RNA的种类不断增长。近期,针对circRNA分子的研究方法,以及高通量测序技术的进步,大量的circRNA在不同物种中被鉴定。有研究表明circRNA呈发育调控、组织/细胞特异表达,并且所有真核生物均存在circRNA,但关于circRNA在牛成肌细胞分化、凋亡方面的报道少之又少。
牛肉是一种营养价值较高的畜肉食品,它具有高蛋白、低脂肪、低胆固醇的特点。骨骼肌主要参与维持机体运动和能量代谢,是肉质研究的重要对象。我们选择秦川牛为研究对象,通过高通量测序技术,鉴定肌肉组织中存在的circRNA,采用生物信息学方法分析差异表达基因,并结合功能验证试验手段,揭示circRNA在肌肉分化、凋亡中的功能及其调控机制,以期解决我国黄牛品种生长速度慢,产肉性能低等缺点,为我国肉牛产业的发展提供理论基础。
研究发现
本研究根据课题组前期的circRNA高通量测序数据筛选出circFGFR4,通过qPCR检测其在不同组织中的表达量,发现circFGFR4在肌肉组织中高表达(见图一)。通过TargetScan和RNAhybrid软件预测发现circFGFR4有18个潜在miR-107结合位点,因此我们选择circFGFR4作为下一步的研究对象。
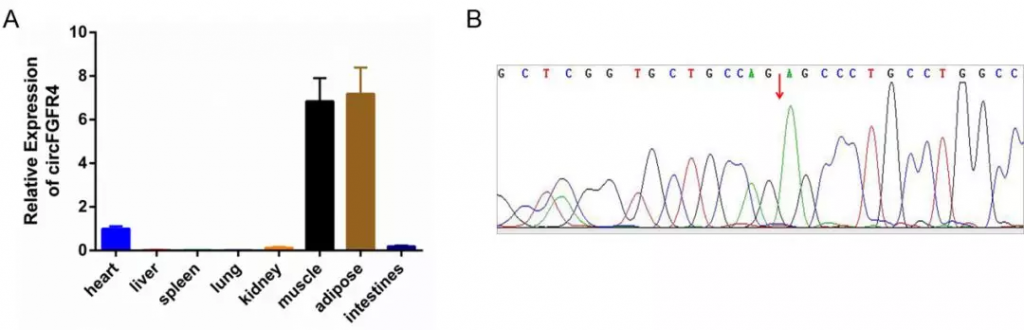
图1 circFGFR4表达的检测
有研究报道,circRNA可作为分子海绵竞争性吸附miRNA,从而调节其下游靶基因的表达。于是我们采用双荧光素酶报告、RNA-RNA pull down对circFGFR4的分子海绵作用进行验证,结果显示circFGFR4能够吸附miR-107,文献报道在牛成肌细胞中Wnt3a是miR-107的一个靶基因。过表达circFGFR4发现Wnt3a的表达量增加(见图2)。
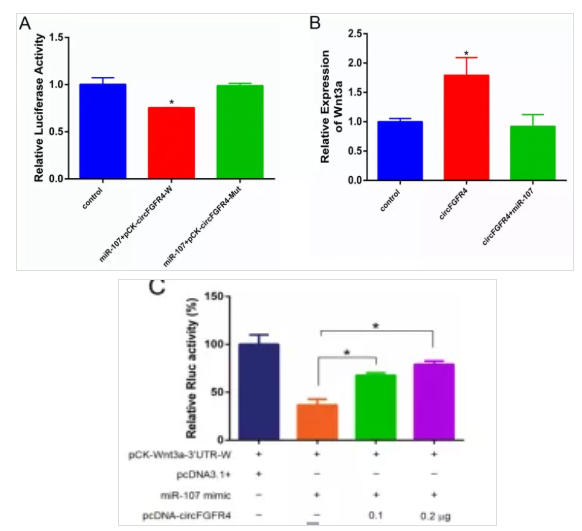
图2 circFGFR4表达分析
以上结果证明,circFGFR4可以竞争性结合miR-107,那么circFGFR4是否通过吸附miR-107影响牛成肌细胞分化?我们做了qPCR、western blot、免疫荧光。结果表明,circFGFR4可以通过吸附miR-107促进牛成肌细胞分化(见图3)。
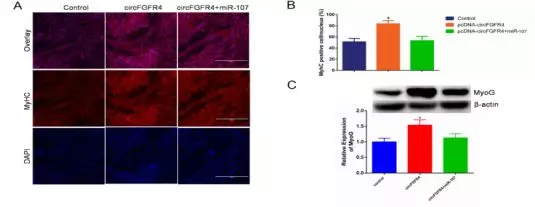
图3 circFGFR4促进肌管形成
已有文献报道miR-107抑制成肌细胞凋亡,那么circFGFR4是否通过吸附miR-107发挥细胞凋亡作用,进一步实验发现circFGFR4可以通过吸附miR-107促进细胞凋亡(见图4)。
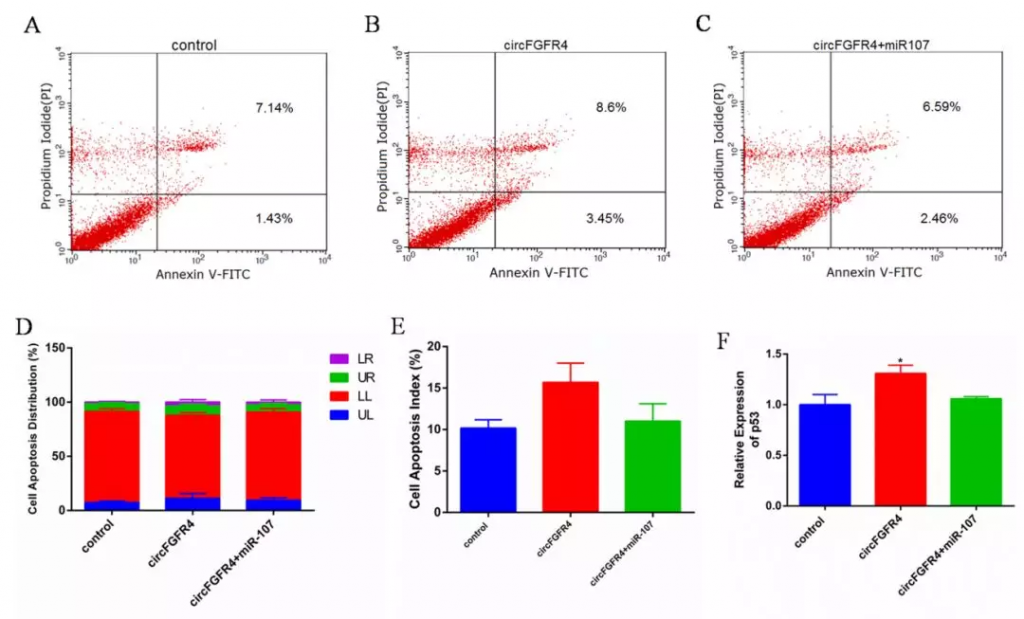
图4 circFGFR4通过吸附miR-107促进细胞凋亡
个人感悟
作为一名硕士研究生,我体会到做实验之前首要要建立清晰的实验思路,其次就是基础知识的积累。当然,一名科研工作者要实现自己的科研梦想,仅有眼光、仅有情怀是不够的;眼光和情怀的落地,还需要奋发、需要执着。
感谢联川
由于LncRNA是非编码RNA家族的一员,而绝大多数lncRNAs的功能是未知的,所以我们选择对LncRNA进行一个测序,在众多测序公司当中我们选择了联川生物不只是因为联川的知名度还因为联川的责任心和对客户的关怀,在方案设计,样品采集和后续的生信分析中都给予大量的热情帮助,对此非常感激。衷心希望联川生物发展的越来越好,同时期待下一次的合作!
本文通讯作者简介
遗传学博士、博士后,教授(二级),现为西北农林科技大学动物遗传育种与繁殖学科、遗传学学科博士生导师、学术带头人、动物科学系主任。国务院政府特殊津贴获得者、全国优秀农业科教工作者、陕西省高等学校教学名师、陕西省师德标兵、西北农林科技大学拔尖人才支持计划入选者、西北农林科技大学“教学名师支持计划”入选者。

参考文献:Li H, Wei X, Yang J, et al. CircFGFR4 Promotes Differentiation of Myoblasts via Binding miR-107 to Relieve Its Inhibition of Wnt3a[J]. Molecular Therapy Nucleic Acids, 2018, 11(C):272-283.





来第一个抢占沙发评论吧!