转自: BioWorld(微信公众号)
2019年4月25日,中科院生化所陈玲玲团队等在 Cell 杂志发表关于环状RNA(circRNA)的最新研究,首次阐述了环状RNA在细胞受病毒感染时的降解机制,及其通过形成分子内双链结构结合天然免疫因子参与天然免疫应答调控的重要新功能,并揭示环状RNA低表达与炎症性自身免疫性病—系统性红斑狼疮(SLE)密切相关。该工作为环状RNA在天然免疫中的重要功能研究奠定基础。
2019年4月29日,曹雪涛院士团队在 Nature Immunology 杂志上发表关于长链非编码RNA(LncRNA)的最新研究。揭示了lncRNAzc3h7a可分别直接结合TRIM25和RIG-I,从而正向调控RIG-I介导的信号通路和抗病毒天然免疫反应。
这两项研究发现了circRNA和LncRNA这两种非编码RNA全新的功能——参与天然免疫应答,抵抗病毒入侵。
circRNA

circRNA(CircularRNA,环状RNA)是一类不具有5‘ 末端帽子和3’ 末端poly(A)尾巴、并以共价键形成环形结构的客观存在于生物体内的非编码RNA分子。1976年,circRNA分子首次被发现,经过30多年的沉寂后,在2013年,Nature 杂志同期发表两篇论文,表明circRNA通过作为miRNA的海绵来调控基因表达,circRNA从此一鸣惊人,并在随后几年时间里迅速成为新一代明星分子。
2019年4月25日,中科院生化所陈玲玲团队、中科院计算生物学研究所杨力团队、上海交通大学医学院附属仁济医院沈南团队合作在Cell 杂志发表题为:Structure and degradation of circular RNAs regulate PKR activation in innate immunity 的研究论文。
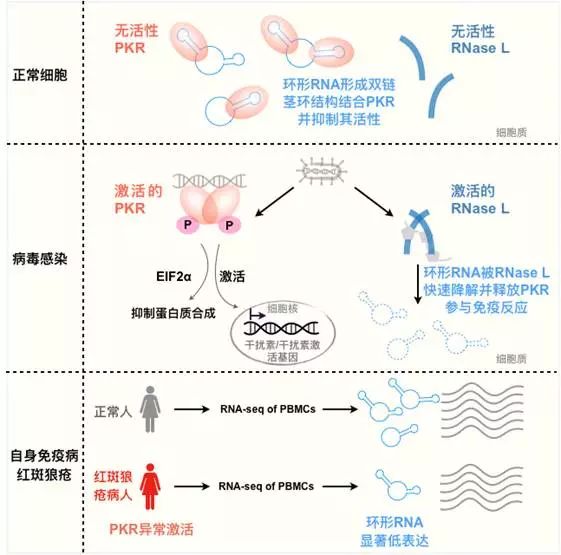
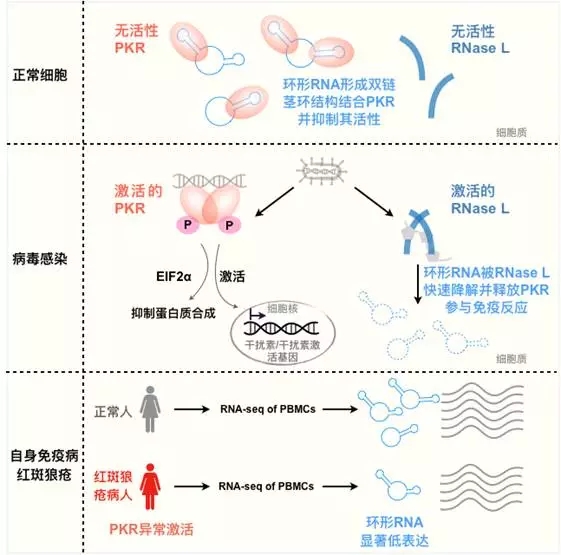
该研究首次阐述了环状RNA在细胞受病毒感染时的降解机制,及其通过形成分子内双链结构结合天然免疫因子参与天然免疫应答调控的重要新功能,并揭示环状RNA低表达与炎症性自身免疫性病—系统性红斑狼疮(SLE)密切相关。该工作为环状RNA在天然免疫中的重要功能研究奠定基础,并为炎症性自身免疫病的发病机制及未来的干预治疗提出了新的思路与潜在靶点。
环形RNA参与抗病毒免疫反应
总的来说,这些发现不仅首次揭示了环状RNA的降解途径及其特殊二级结构特征,并提示环状RNA发挥免疫调控的全新功能。相关研究进展为环状RNA代谢和功能研究奠定了重要基础,也为红斑狼疮等自身免疫病的临床诊断和治疗提供了新思路。
LncRNA

注:该研究第一署名单位为浙江大学免疫研究所
LncRNA(Long non-coding RNA),是长度大于200个核苷酸的非编码RNA,LncRNA起初被认为是基因组转录的“噪音”,是RNA聚合酶II转录的副产物,不具有生物学功能 。然而,1991年,Nature 等杂志刊文证实 Xist 参与X染色体失活的调控。2007年,张元豪在 Cell 发表论文,发现 LncRNA-HOX 的功能。此后越来越多的研究表明,LncRNA在众多生命活动过程中发挥重要作用,LncRNA开始引起人们广泛的关注。再加上二代测序技术的发展,大量 LncRNA 被发现,LncRNA相关研究迅速爆发。
2019年4月29日,曹雪涛院士团队在 Nature Immunology 杂志上发表题为:The long noncoding RNA Lnczc3h7a promotes a TRIM25-mediated RIG-I antiviral innate immune response 的研究论文。
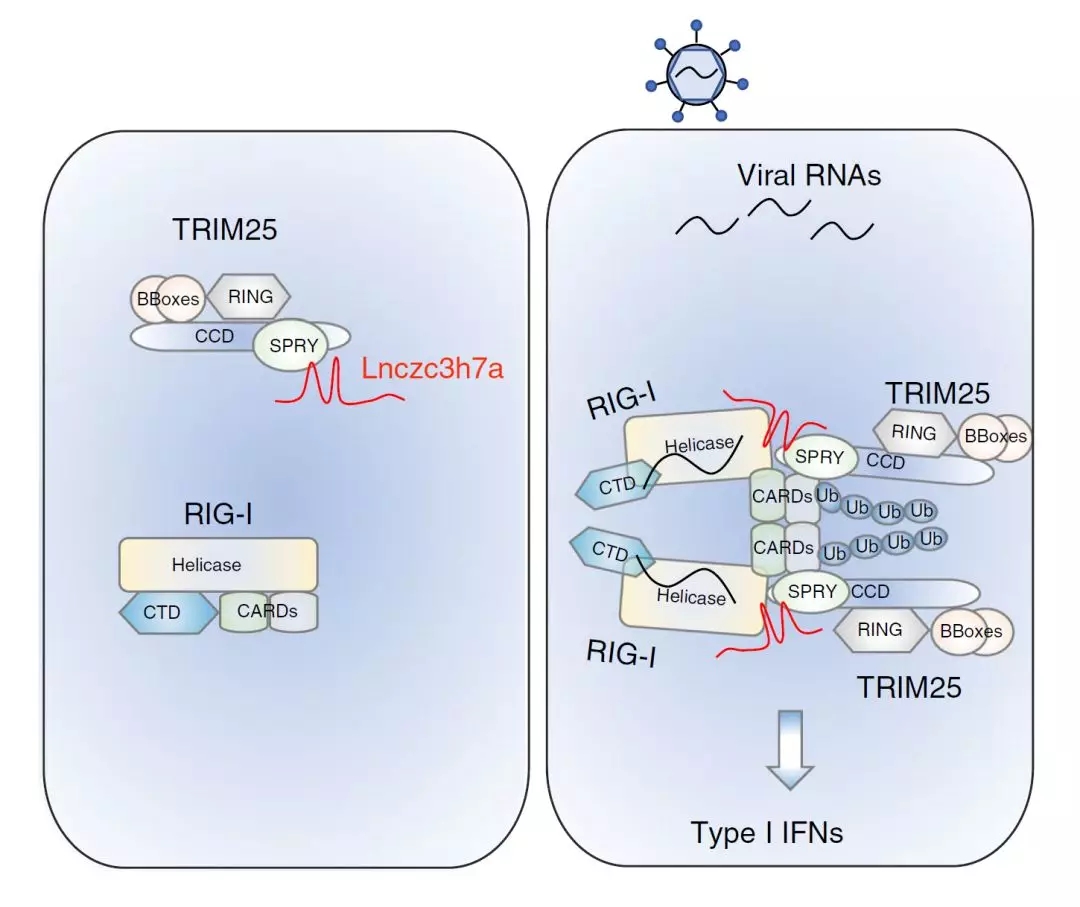
该研究发现了一种新的长非编码RNA(Lnczc3h7a),它与TRIM25结合并促进RIG-I介导的抗病毒先天免疫反应。在机制上,Lnczc3h7a与TRIM25和活化的RIG-I结合,在病毒感染的早期阶段用作稳定RIG-I-TRIM25复合物的分子支架。 Lnczc3h7a促进TRIM25介导的RIG-1的K63连接的泛素蛋白化,从而促进下游信号转导。 研究结果表明,宿主RNA可以增强先天免疫传感器对外来RNA的反应,确保有效的抗病毒防御。
长非编码RNA(lncRNA)通过不同的机制在免疫细胞发育和免疫反应中发挥重要作用,包括信号、诱饵、指导或支架作用。先前已经发现了通过直接结合靶蛋白而参与免疫细胞发育和病毒感染的几种lncRNA,例如,lnc-DC通过直接结合促进STAT3磷酸化,因此是树突细胞分化所必需的。然而,在先天免疫应答的早期阶段与关键先天信号分子相互作用以增强抗病毒先天免疫应答的lncRNA需要进一步鉴定。
该研究发现了一种新的lncRNA:Lnczc3h7a,其与TRIM25和活化的RIG-I结合以稳定TRIM25-RIG-I相互作用。Lnczc3h7a在抗病毒反应的早期阶段作为这种相互作用的分子支架,增强了RIG-I和下游信号传导的K63连接泛素化。结果,Lnczc3h7a增加I型IFN产生并支持针对RNA病毒感染的更有效的先天免疫应答。
这些研究结果揭示了天然免疫中lncRNA的一个新的调控机制。揭示了以前未被认可的自身RNA在早期加强先天反应以消除非自身RNA的作用,为预防和治疗传染病提供了新的策略和目标。
论文链接:
http://sci-hub.tw/10.1016/j.cell.2019.03.046
https://www.nature.com/articles/s41590-019-0379-0



来第一个抢占沙发评论吧!