转自: 科研者言(微信公众号)
环状RNA的定义是什么?circRNAs(Circular RNAs,环形RNA分子)是一类不具有5' 末端帽子和3' 末端poly(A)尾巴、并以共价键形成环形结构的非编码RNA分子。它们通过pre-mRNA在细胞核内backsplicing形成环状,与之相对的,就是具有5' 末端帽子和3' 末端poly(A)尾巴的RNA分子了?那是什么呢?就是mRNA、lncRNA这些两端开放的RNA分子了。
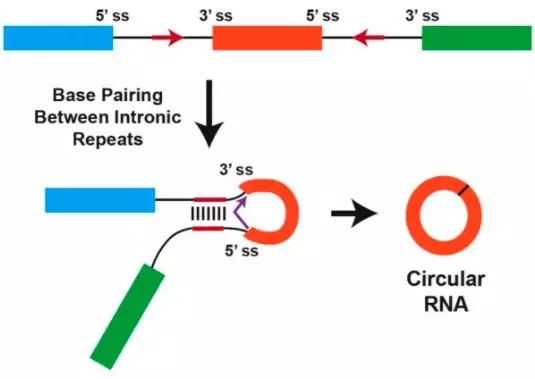
circRNA在发表的高分文章中可大致分为三类机制:ceRNA(吸附miRNA,作为海绵)、可编码翻译成为短多肽、结合功能蛋白调控其胞内功能。
文章总数统计数字
那么今天我们总结了9个推荐的circRNA研究思路,希望对童鞋们有所启发,如下:
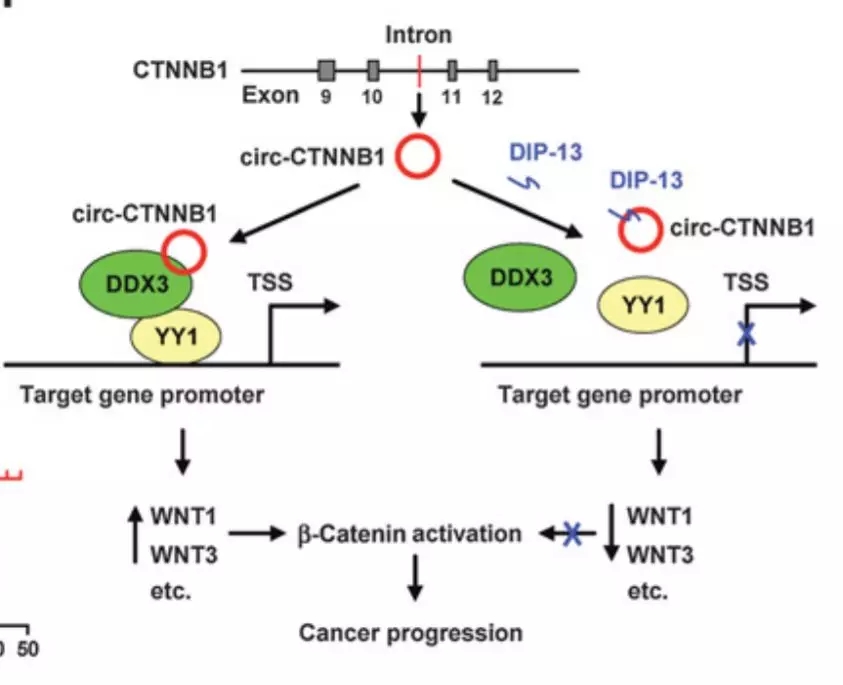
1.Cis-Acting circ-CTNNB1 Promotes β-Catenin Signaling and Cancer Progression via DDX3-Mediated Transactivation of YY1.
Cancer Res9.131区. 2019 Feb

分子机制:这篇文章介绍顺式调控作用的circRNA,由β-catenin(基因CTNNB1)转录因子7(β-catenin (CTNNB1)/transcription factor 7-like 2)促进转录后筛选表达差异的circRNA,筛选到一个由CTNNB1基因内含子转录产生的circ-CTNNB1,其在细胞核内表达水平较高,在癌组织以及肿瘤细胞系中也较高,而且和多种肿瘤的差的预后相关。细胞功能实验发现circ-CTNNB1可激活β-catenin 的表达,以及肿瘤细胞的增殖侵袭和转移。当敲减Circ-CTNNB1的表达,以及使用特异性抑制性多肽可抑制Circ-CTNNB1和DDX3的物理性结合。分子机制上,Circ-CTNNB1可结合DEAD-box polypeptide 3 (DDX3),促进DDX3和Yin Yang 1(YY1)的物理性结合,导致了YY1的反式调控激活下游的基因,其中就包括Wnt/β-catenin信号通路的相关基因。
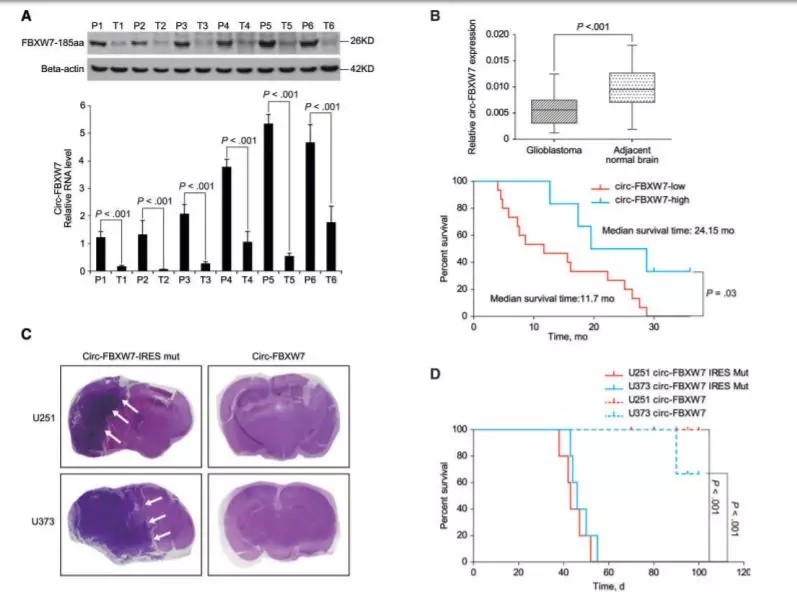
2.Novel Role of FBXW7 Circular RNA in Repressing Glioma Tumorigenesis.
1区11.238J Natl Cancer Inst. 2018 Mar 1

分子机制:恶性胶质瘤10对样本进行测序,细胞株包括U251和U373进行体外功能以及分子机制实验,测序结果发现Circ-FBXW7在肿瘤样本中异常低表达,且其低表达和恶性胶质瘤差的预后相关,进一步的体内外功能实验证明,高表达Circ-FBXW7显著抑制U251和U373细胞的增殖侵袭和转移。进一步的生信分析发现Circ-FBXW7具备编码多肽链的能力,叫做FBXW7-185aa ,当单独在体外、体内实验中,过表达或者敲减FBXW7-185aa时,结果表明是FBXW7-185aa而不是 Circ-FBXW7本身发挥着抑制肿瘤恶性生物学行为的作用。分子机制上FBXW7-185aa使得c-myc癌蛋白的稳定性变差,半衰期变短,抑制去泛素化水解酶Usp28对于c-myc癌蛋白稳定性的调控。
3.A novel FLI1 exonic circular RNA promotes metastasis in breast cancer by coordinatelyregulating TET1 and DNMT1.
1区13.214Genome Biol. 2018 Dec 11

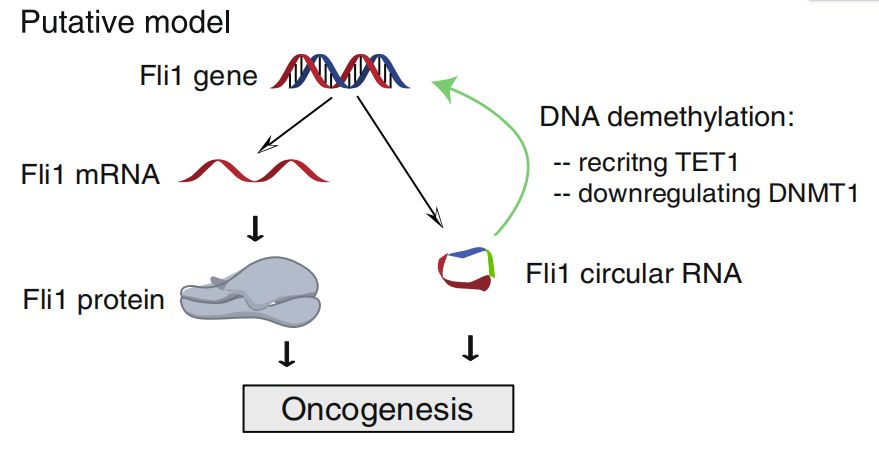
分子机制:FLI1(Friend白血病病毒插入位点l)是一个癌基因驱动子,可促进实体肿瘤的增殖和侵袭。作者首先实验发现FLI1在乳腺癌的各个分期以及转移阶段,均持续高表达。通过免疫共沉淀技术测序发现FLI1启动子区以及外显子去可转录出一个circRNA,命名为FECR1。体外细胞功能实验FECR1独立促进MDA-MB231 breast cancer cell的增殖和侵袭。机制上发现,FECR1可通过正反馈回路介导FLI1启动子区低甲基化修饰,促进了FLI1的转录,原来FECR1可顺式调控FLI1而招募TET1蛋白,其发挥DNA脱甲基的作用,进行启动子区的去甲基化作用。作用机制如下。
备注:TET(ten-eleven translocation)蛋白家族是一组能够调节各种表观遗传反应的DNA脱甲基酶,可将5-甲基胞嘧啶(5mC)转化为5-羟甲基胞嘧啶(5hmC)。该过程是DNA去甲基化的1个必要阶段。5hmC可在活性转录基因起始位点和Polycomb抑制基因启动子延伸区域富集。TET蛋白包括3个成员TET1、TET2和TET3,均属于α-酮戊二酸和Fe2+依赖的双加氧酶,其催化涉及氧化过程。
4.Structure and Degradation of Circular RNAs Regulate PKR Activation in Innate Immunity.
Cell31.3981区. 2019 May 2

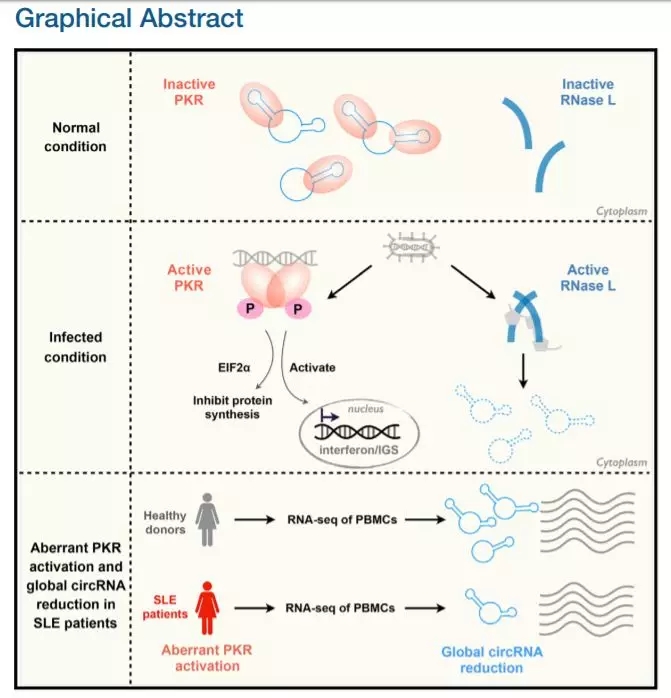
分子机制:本文的circRNA研究的是和固有免疫相关。本文作者测序SLE红斑狼疮病人或者是病毒感染的PBMC细胞和正常人的PBMC细胞,发现两种状态下(病理和正常),细胞内的circRNA表达谱变化较大,所有的circRNA都会被RNase L大量降解,而这个RNase L正是在在dsRNA激活的PKR激活时发生的事件。在正常情况下,circRNA倾向于形成16-26 bp大小的RNA双聚合体,可发挥PKR的抑制剂,而PKR正是机体固有免疫激活的效应分子。而当发生病毒感染或者自体免疫疾病时,PBMC中的circRNA被降解,而PKR受体则被大量磷酸化激活。功能实验时发现,发现在PBMC以及T-cell中过表达具有dsRNA结构的circRNA时,其可结合抑制PKR,减弱了PKR激活的级联放大效应,提供了一种全新的circRNA参与自体免疫疾病以及病毒感染导致机体发病的研究。
5.RNA Circularization Diminishes Immunogenicity and Can Extend Translation Duration In Vivo.
Mol Cell14.2481区. 2019 May 2
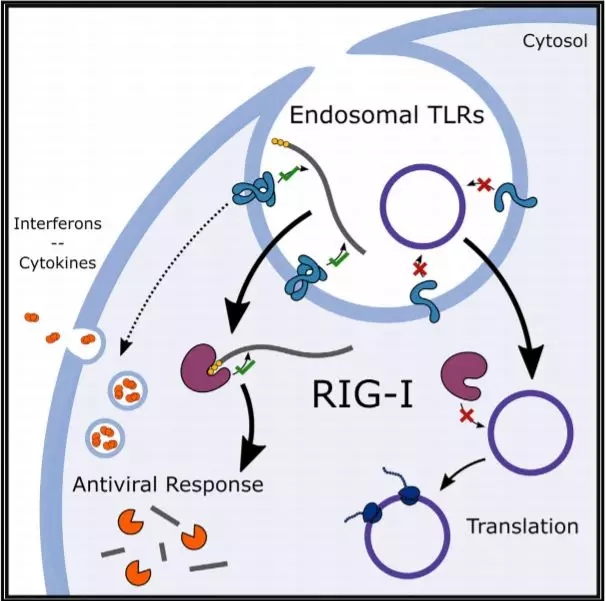
分子机制:自然界中存在很多的RNA病毒,机体为有效抵御这些病毒的感染,进化出了复杂的免疫系统,其中针对RNA分子的识别受体是激活相关免疫机制的触发器。已知RNA感受器包括RIG-I,TLR-3/7/8等分子,它们可以识别不同的RNA或其降解产物。在利用长链RNA进行外源基因导入和表达的实验中,常引入特殊的RNA修饰以降低这些RNA感受器分子介导的免疫效应,这些修饰包括假尿苷修饰,N1-甲基假尿,5-甲氧基尿苷(5moU)修饰等等。本文作者报道了未经修饰的外源的circRNA可以绕过小鼠机体中含有RIG-I以及TLR成分的细胞,避免激活免疫反应,但是线性的RNA可以激活强烈的免疫反应。而在体外的功能实验显示,同样的环状的circRNA的免疫刺激反应更弱。
体外环化的circRNA可在体内翻译:为分析高纯度的体外环化circRNA能否在体内被有效翻译,作者在小鼠体内进行了分析。作者构建了环化的人促红细胞生成素的circRNA和带N1-甲基假尿修饰的线性mRNA,体外细胞实验表明两者翻译效率相当。注射小鼠后分析血清中游离分子的半衰期,表明circRNA存在的时间更持久。小鼠体内能够检测到注射体外环化的circRNA的翻译产物,表明高纯度的体外环化circRNA可以在体内实现有效,稳定的蛋白表达。作者最后还尝试脂质体进行体外环化circRNA的包裹和体内给药,结果表明体外环化的高纯度circRNA能够兼容纳米脂质体载体。
6.Loss of Super-Enhancer-Regulated CircRNA Nfix Super-Enhancer-Regulated CircRNA Nfix Induces Cardiac Regeneration After Myocardial Infarction in Adult Mice.
Circulation18.881区. 2019 Apr 5

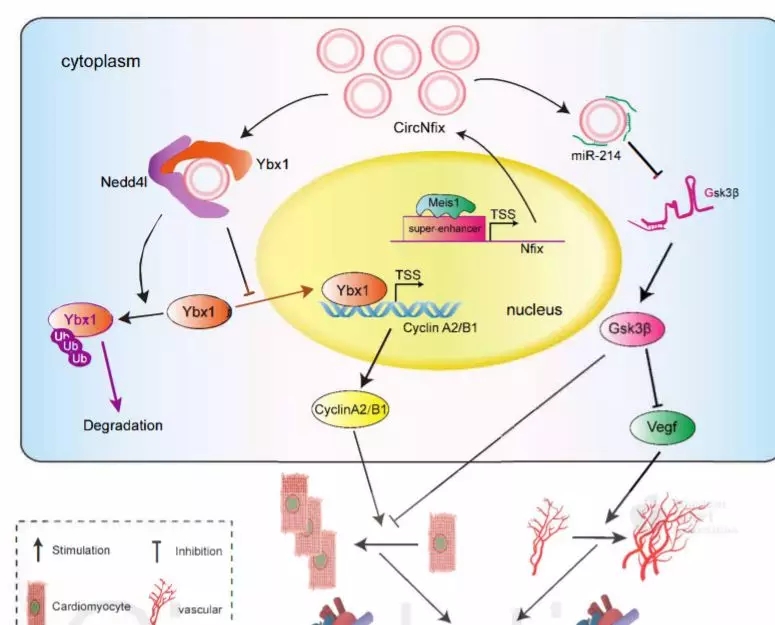
分子机制:本文作者通过测序发现一个circRNA,名叫circNfix,可以被超级启动子(Super-enhancer)调控,其在人类、大鼠、小鼠的心脏中高表达。而转录因子Meis1被发现可结合该circNfix的SE序列上,增加其表达水平。在体内外实验中发现,当把circNfix敲减后,心肌细胞增殖促进,否则反之。进一步发现敲减circNfix可促进血管生成,而抑制心脏缺血后的心肌细胞的凋亡,减弱心脏功能失调,促进了病人的预后。机制上,circNfix促进了YBX1和NEDD4I(E3泛素连接酶),引起了YBX1的泛素化降解,抑制了cyclin蛋白A2以及B1的表达。另外还有一条分子机制,那就是其可吸附miR-214,从而促进了Gsk3β的表达,进一步抑制了WNT/β-catenin通路,抑制了心肌细胞的增殖,促进其凋亡。
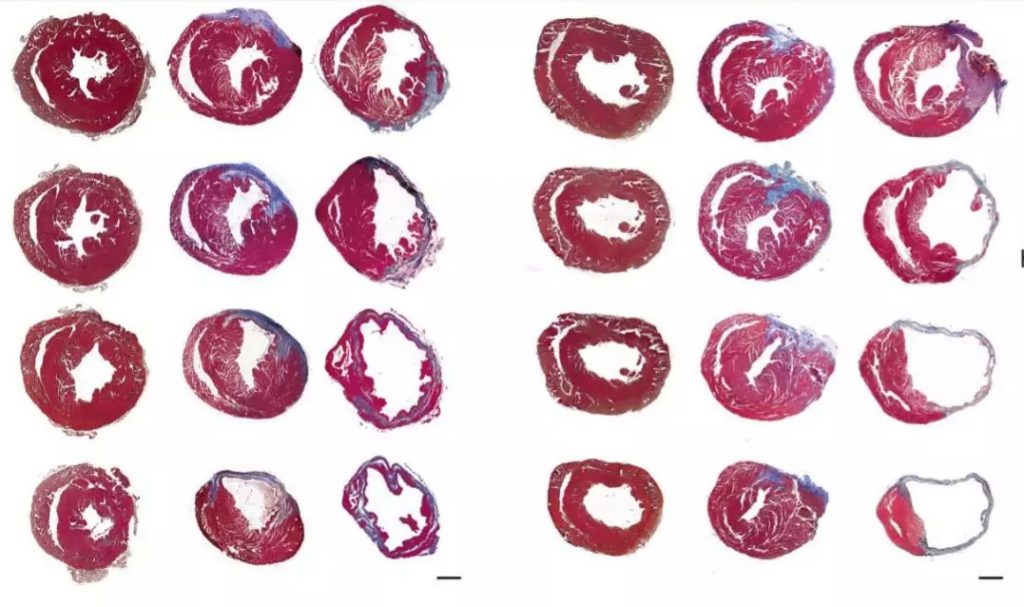
7.Exosomal circRNA derived from gastric tumor promotes white adipose browning by targeting the miR-133/PRDM16 pathway.
Int J Cancer7.361区4. 2019 May 15

分子机制亮点:不仅仅是ceRNA,还有热点外泌体。本文通过对胃癌病人的血液外泌体进行测序,结合统计学分析发现ciRS-133和白色脂肪组织变成褐色脂肪组织有相关性。通过进一步的细胞培养和测序发现,胃癌细胞可分泌携带了ciRS-133的外泌体(exosome),在体外和体内功能实验中发现,敲减掉ciRS-133的脂肪细胞前体细胞,可抑制其向褐色脂肪细胞分化。分子机制上,ciRS-133通过吸附抑制miR-133,促进了靶基因PRDM16的表达,在这个代谢方向里,PRDM16水平升高可使白色脂肪转为浅棕色脂肪是一个经典知识点,所以这篇文章通过将上游创新点结合明星基因PRDM16,形成了完整的创新机制。
背景:恶病质(cachexia)亦称恶液质。表现为极度消瘦,皮包骨头,形如骷髅,贫血,无力,完全卧床,生活不能自理,极度痛苦,全身衰竭等综合征。多由癌症和其他严重慢性病引起。可看作是由于全身许多脏器发生障碍所致的一种中毒状态。此症的发生多指机体处于严重的机能失调状态。
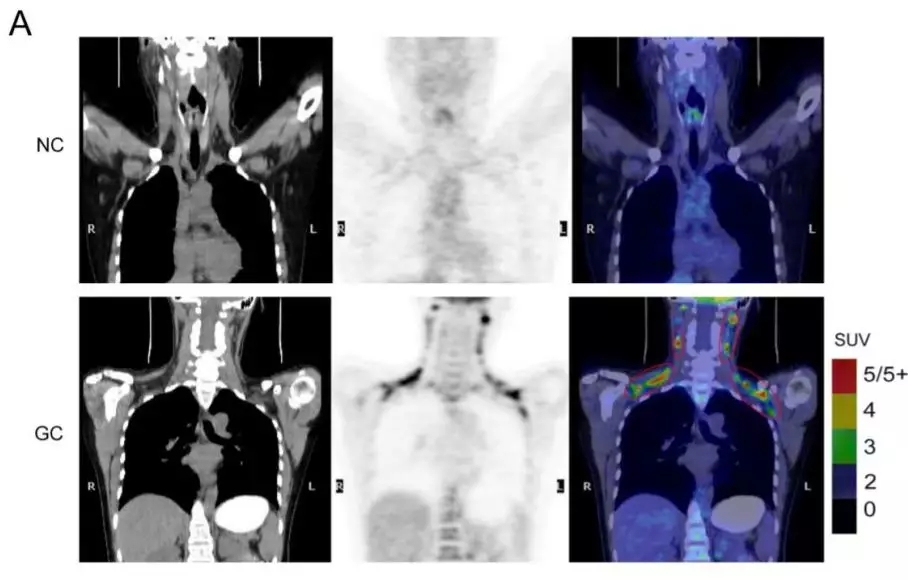
8.Translation of the circular RNA circβ-catenin promotes liver cancer cell growth through activation of the Wnt pathway.
Genome Biol13.2141区1. 2019 Apr 26
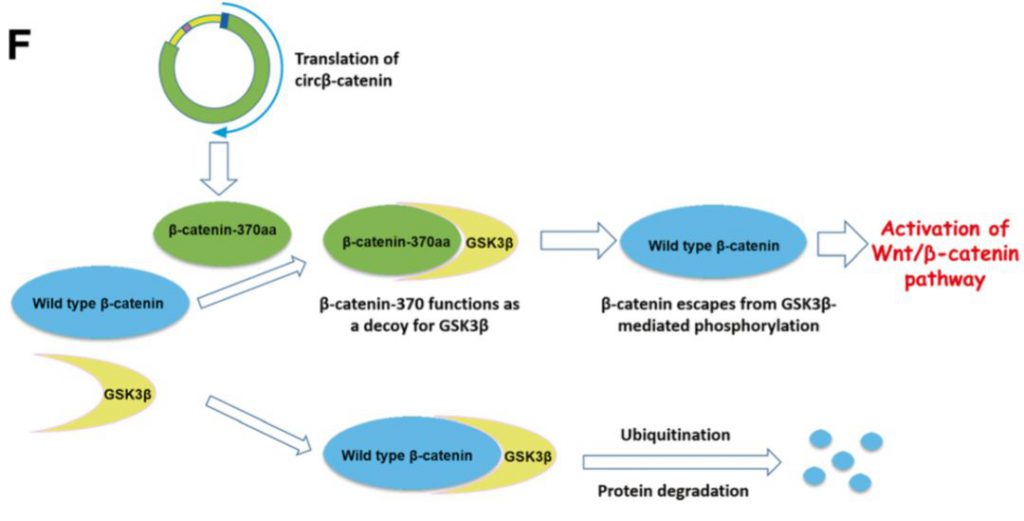
分子机制:首先检测发现Circβ-catenin是一个更多分布在细胞质中的一个circRNA,尤其在肝癌组织中高表达。敲减掉Circβ-catenin后,可在细胞内和动物体内抑制肝癌细胞的增殖以及肿瘤的大小,抑制其生物学恶性行为,而在信号通路的检测上发现其和β-catenin的表达正相关,但是不改变其mRNA水平,只改变其蛋白水平。但发现Circβ-catenin可编码多肽,命名为β-catenin-370aa多肽,这个多肽是β-catenin同型异构体,也就是结构上类似,经过测序发现Circβ-catenin其实是β-catenin基因转录本环化形成的circRNA,那么这个多肽即可结合GSK3β,抑制其磷酸化β-catenin以及泛素化降解的经典途径,这是另类的牺牲自己,拯救兄弟的机制。
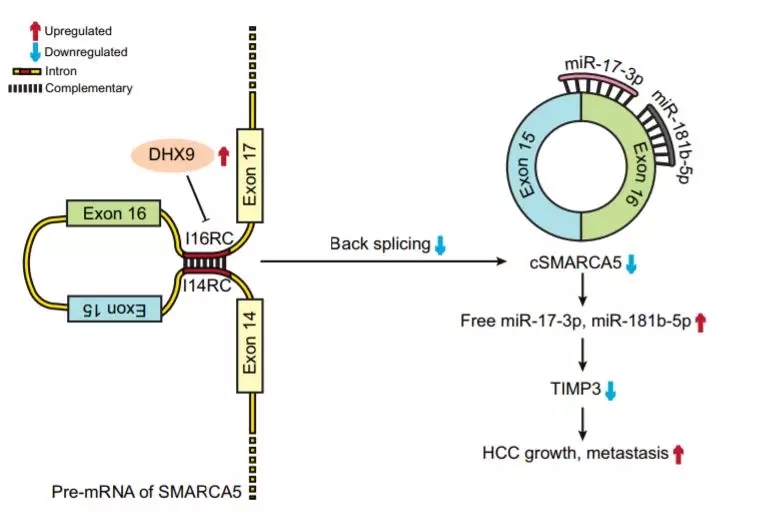
9.Circular RNA cSMARCA5 inhibits growth and metastasis in hepatocellular carcinoma.
J Hepatol14.9111区30. 2018 Jun

分子机制:这个分子机制还是ceRNA,但是是双miRNA,也就是一个circRNA可吸附两种miRNA的机制,在课题上也算是创新的一种。通过高通量测序,分析得到cSMARCA5在肝癌组织中呈现低表达,其被高表达的DExH-Box Helicase 9抑制,通过独立的分享因子分析,低表达的cSMARCA5肝癌换着预后更差(OS、RFS都差),肿瘤的侵袭性更强,体内体外实验发现高表达cSMARCA5之后肝癌细胞的增殖和侵袭能力变弱,机制上发现原来其可同时吸附miR-17-3p and miR-181b-5p两个miRNA,阻止它们靶向降解TIMP3蛋白(百度一下该蛋白,会发现其属于一个抑癌基因,明星基因)



来第一个抢占沙发评论吧!