英文标题:Circular RNA circNHSL1 promotes gastric cancer progression through the miR-1306-3p/SIX1/vimentin axis
中文标题:环状RNA circNHSL1通过miR-1306-3p/SIX1/vimentin调控轴促进胃癌进程
发表期刊:Molecular Cancer
影响因子:10.679
发表时间:2019年8月
作者单位:上海交通大学附属第一人民医院,上海交通大学医学院
研究技术:全转录组测序(欧易生物提供)
研究背景
胃癌是全球第五大最常见的癌症,也是导致世界范围内癌症相关死亡的第三大原因。胃癌作为最常见的消化道恶性肿瘤之一,其在早期难以诊断,且进展迅速,多数患者在晚期时才被诊断出来,5年生存率低于30%。而导致晚期胃癌预后不良的主要原因就在于其转移性。因此阐明胃癌发展、转移的分子机制,发现早期诊断和治疗的新型分子靶点迫在眉睫。
circRNA是一种新兴起的非编码RNA,近年来被发现在多种分子机制中发挥作用,如作为microRNA海绵、翻译蛋白和结合RNA结合蛋白等。其中miRNA海绵是circRNA在肿瘤的发生发展中最常见的作用。尽管在胃癌中已有几种circRNA被报道,但很少有肿瘤转移相关的circRNA及其功能和分子机制被报道。
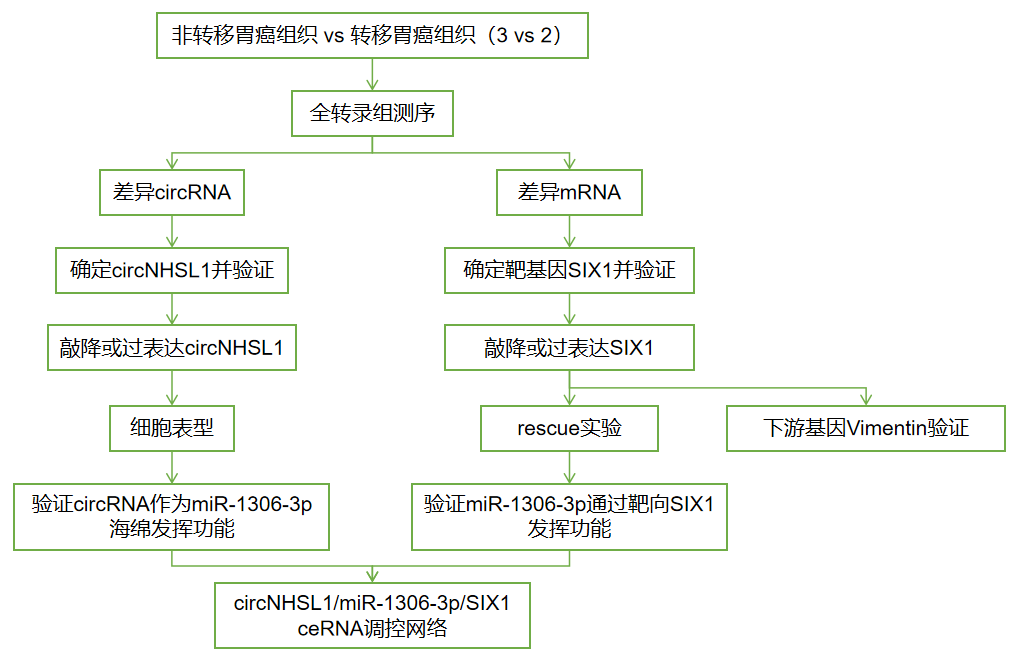
技术路线
研究结果
1、circNHSL1在胃癌组织中上调,并与疾病进程和预后不良相关
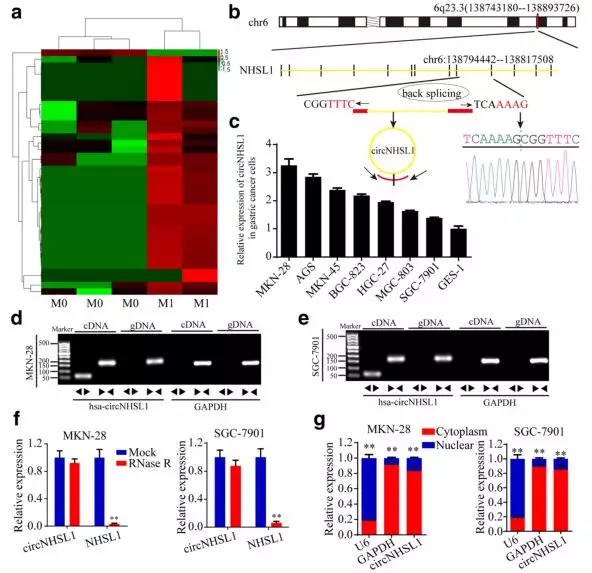
作者通过对3例未转移胃癌组织和2例转移胃癌组织进行全转录组测序,筛选出37个在转移胃癌组织中显著上调的circRNA,1个下调circRNA(Fig 1a)。从中选取了上调最多的circNHSL1,设计了divergent和convergent两对引物,通过一代测序(Fig 1b)、以cDNA和gDNA为模板进行PCR(Fig 1d,e)、RNase R处理(Fig 1f)的方法验证circNHSL1成环,并在不同的胃癌细胞系及正常人胃上皮细胞系中验证其表达量,发现在多种胃癌细胞系中circNHSL1表达显著高于正常细胞系(Fig 1c)。
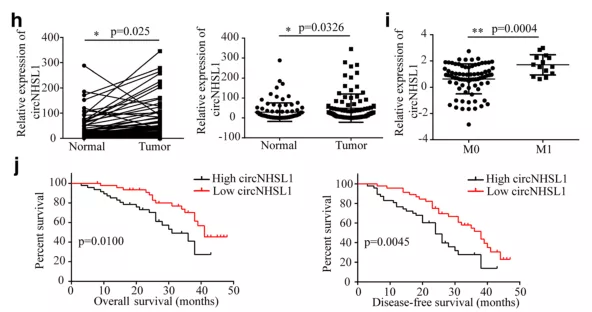
随后作者对93对冰冻的胃癌组织及正常组织进行qPCR定量,发现癌症组织中circNHSL1表达显著升高(Fig 1h),并且M1期胃癌组织中的表达显著高于M0期(Fig 1i),通过Kaplan-Meier生存分析发现,高表达circNHSL1的病人的总体生存期及无病生存期显著低于低表达病人(Fig 1j)。
Fig 1. circNHSL1在胃癌组织中表达上调,与胃癌的进展及预后不良相关
2、circNHSL1体外促进胃癌细胞的迁移和侵袭
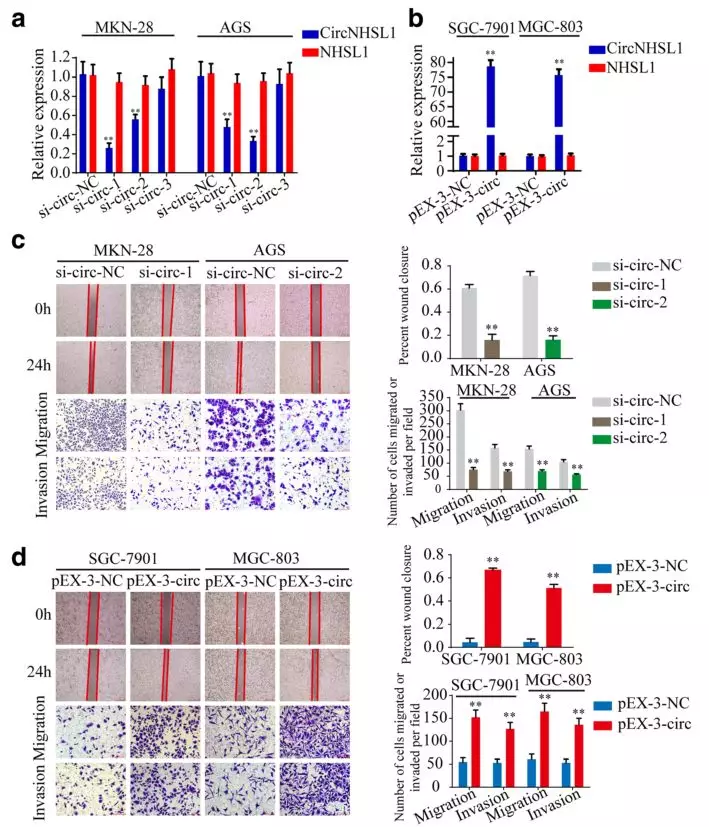
作者在高表达circNHSL1的胃癌细胞系中敲降circNHSL1(Fig 2a),在低表达的胃癌细胞系中过表达circNHSL1(Fig 2b),通过wound healing和transwell实验,发现敲降circNHSL1后,胃癌细胞的迁移、侵袭能力显著降低(Fig 2c),过表达后呈现相反的结果(Fig 2d),这说明circNHSL1在体外能够促进胃癌细胞的迁移和侵袭。
Fig 2. circNHSL1体外促进胃癌细胞的迁移和侵袭
3、circNHSL1通过SIX1基因促进胃癌的进程
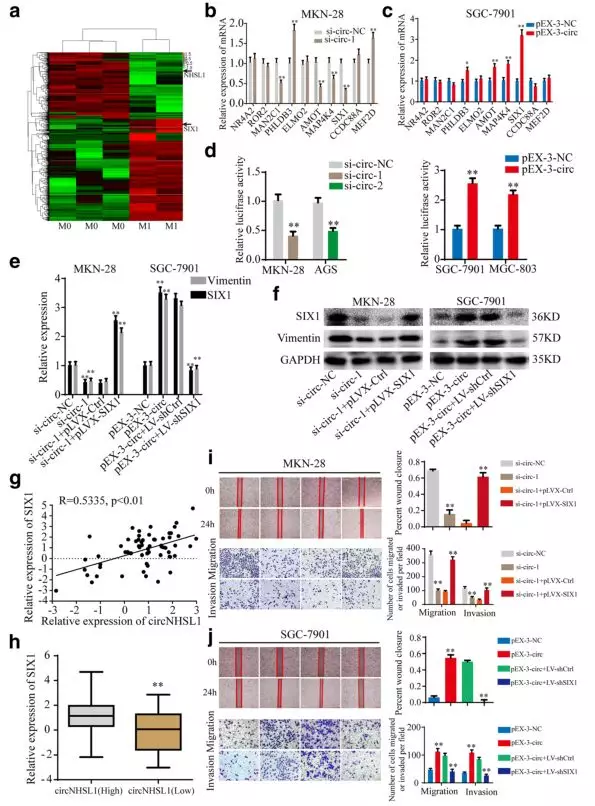
作者通过全转录组测序,筛选到胃癌转移相关的mRNA,选取其中top10的上调基因进行验证(Fig 3a)。MAP4K4和SIX1的表达同时在两个敲降circNHSL1的细胞系中显著下调(Fig 3b,d),而AMOT和SIX1同时在两个过表达circNHSL1的细胞系中显著上调(fig 3c,d),并且发现胃癌组织中SIX1与circNHSL1的表达呈正相关(Fig 3g,h),因此作者猜测SIX1为circNHSL的下游靶基因。他们通过挽救实验,即在敲降circNHSL1的同时过表达SIX1,以及过表达circNHSL1的同时敲降SIX1(Fig 3e,f),发现SIX1可以挽救circNHSL1表达量改变导致的细胞表型(Fig 3i,j),这说明circNHSL1通过SIX1促进胃癌的进程。
Fig 3. circNHSL1通过SIX1基因促进胃癌的进程
4、SIX1通过转录调节Vimentin促进胃癌进程
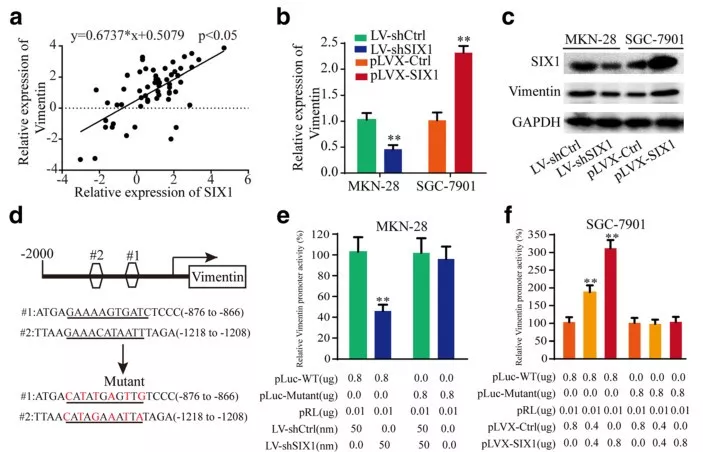
SIX1是一种转录因子,作者通过软件预测了SIX的靶基因,发现在Vimentin基因启动子上存在两个潜在的SIX结合位点(Fig 4d),而Vimentin是一种与肿瘤转移相关的蛋白。作者随后在胃癌组织中发现两者的表达量呈正相关(Fig 4a),敲降或过表达SIX1在mRNA及蛋白水平上改变了Vimentin的表达(Fig 4b, c)。最后作者通过荧光素酶报告实验验证了SIX1与Vimentin的启动子存在相互作用。
Fig 4. SIX1转录调节Vimentin的表达
5、circNHSL1作为ceRNA,通过与SIX1竞争结合miR-1306-3p,促进胃癌进程
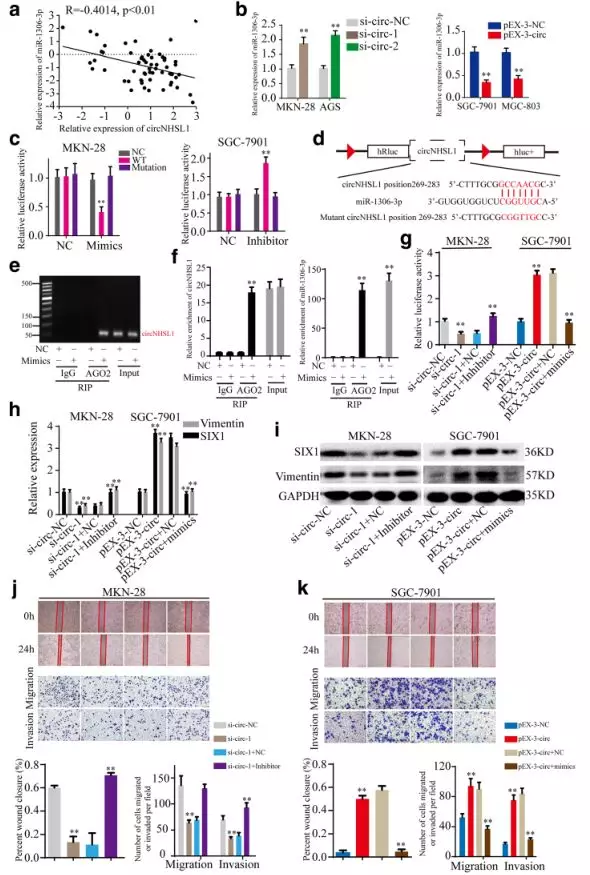
作者通过数据库预测发现circNHSL1与SIX1具有共同的miR-1306-3p结合元件且预测得分高,因此以miR-1306-3p为对象,研究circNHSL1调控的ceRNA网络。作者发现在胃癌组织中,miR-1306-3p的表达量与circNHSL1呈负相关(Fig 5a),在胃癌细胞中敲降或过表达circNHSL1会导致miR-1306-3p的表达上升或下降(Fig 5b)。随后,作者通过荧光素酶报告实验(Fig 5c,d),以及anti-AGO2 RIP实验(Fig 5e, f),验证了circNHSL1与miR-1306-3p之间存在直接的互作关系。为了验证miR-1306-3p在胃癌进程中起到的作用,作者又通过miR-1306-3p的抑制剂和mimics进行了挽救实验,发现miR-1306-3p能够挽救circNHSL1对胃癌细胞的作用(Fig 5h-k)。
Fig 5. circNHSL1通过充当miR-1306-3p的海绵促进胃癌进程
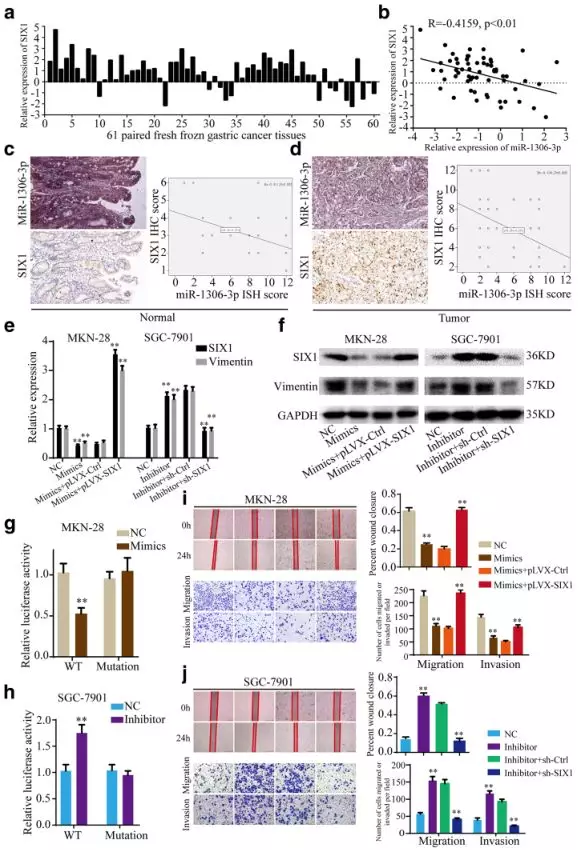
之后作者为验证miR-1306-3p与SIX1的互作关系,先通过定量PCR和原位杂交技术,验证miR-1306-3p与SIX1的表达呈负相关(Fig. 7b-d),过表达或抑制miR-1306-3p可以显著改变SIX1及Vimentin的mRNA和蛋白水平(Fig. 7e, f),通过荧光素酶报告实验验证了miR-1306-3p与SIX1存在直接互作关系(Fig. 7g, h),最后通过挽救实验发现,miR-1306-3p能够挽救SIX促进的胃癌进程(Fig. 7i, j)。
Fig 7. miR-1306-3p通过直接靶向SIX1抑制胃癌进程
综上,作者阐明了circNHSL1/miR-1306-3p/SIX1 ceRNA调控网络调控胃癌的进程。
6、miR-1306-3p在胃癌组织中表达下调,并且与胃癌的进展及预后不良有关
作者通过原位杂交技术检测了miR-1306-3p在胃癌组织及其配对正常组织中的表达(Fig 6a),发现相较于正常组织,其在胃癌组织的表达出现下调(Fig. 6b),并且与胃癌TNM分期、分化程度具有显著的关系(Fig. 6c-f),经Kaplan-Meier生存分析,发现低表达miR-1306-3p的患者预后较高表达miR-1306-3p的患者差(Fig. 6g, h)。
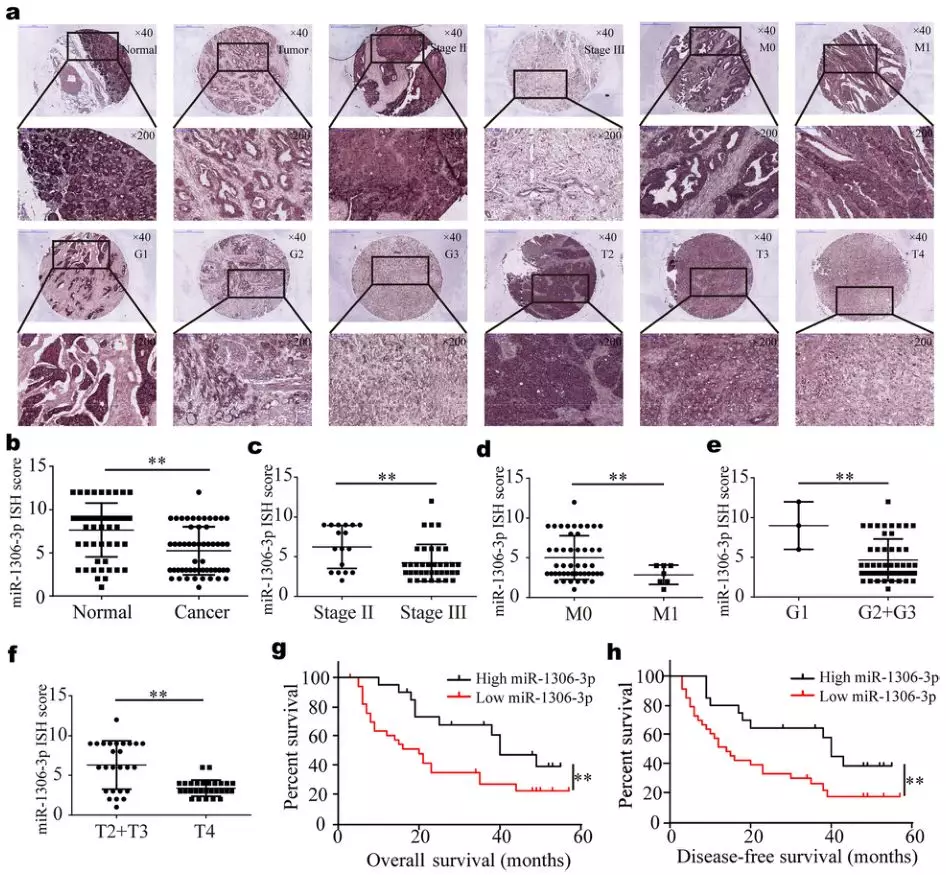
Fig. 6 miR-1306-3p在胃癌组织中表达下调,并且与胃癌的进展及预后不良有关
7、circNHSL1促进胃癌细胞在体内的生长和转移
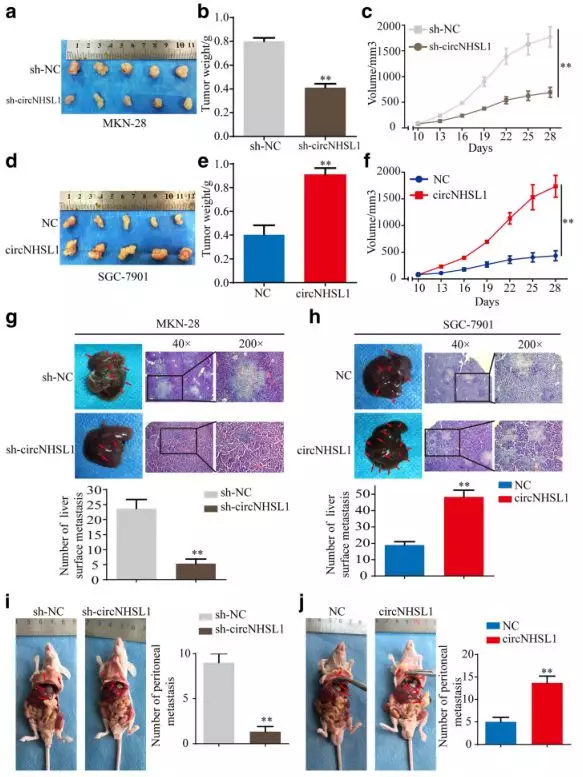
作者通过异种移植,在小鼠皮下注射敲降或过表达circNHSL1的胃癌细胞,发现敲降circNHSL1的胃癌细胞在小鼠体内生长的体积和质量显著降低(Fig. 8a-c),而过表达circNHSL1的胃癌细胞呈现相反的表型(Fig. 8d-f)。此外,作者通过体内肝转移和腹膜转移实验,证实了circNHSL1能够促进胃癌细胞在小鼠的肝及腹膜中的转移(Fig 8g-j)。
Fig. 8 circNHSL1促进胃癌细胞在体内的生长和转移
研究结论
作者通过全转录组测序技术,发现了一种与胃癌转移相关的新型circRNA——circNHSL1,其在胃癌组织中高表达,且与患者的预后不良相关。通过体内外功能研究验证了circNHSL1能够促进胃癌细胞的侵袭和转移,促进胃癌进程。经过一系列的机制研究,作者阐明了circNHSL1可以作为一种竞争内源性RNA(ceRNA),通过与SIX1竞争结合miR-1306-3p,间接调控SIX1的表达水平,从而调控胃癌进程。同时,研究发现circNHSL1和miR-1306-3p均有望成为胃癌预后的biomarker,为胃癌的诊断和治疗提供了新的分子靶点。
参考文献
Zhu Z, Rong ZY, et al. Circular RNA circNHSL1 promotes gastric cancer progression through the miR-1306- 3p/SIX1/vimentin axis. Molecular Cancer. 2019, 18:126.





来第一个抢占沙发评论吧!