来源:类器官星球
2024年5月,南方科技大学蒋兴宇教授团队在期刊《Nature Communications》(IF:16.6)在线发表题为:Three-dimensional liquid metal-based neuro-interfaces for human hippocampal organoids 的高水平研究论文。
论文摘要
由人类诱导多能干细胞(hiPSC)衍生的人类海马体类器官(hHO)已成为研究神经退行性疾病(如精神分裂症和阿尔茨海默病)的理想模型。然而,使用商用多电极阵列(MEA)以非侵入方式获取这些自由浮动有机体的电信息仍然是一项挑战。由于通道数量有限,最近开发的3D多电极阵列只能获取少量神经信号。在此,我们报告了一种将基于液态金属-聚合物导体(MPC)的网状神经接口与hHO相结合的海马半球类器官(cyb-organoid)平台。网状MPC(mMPC)集成了128个通道的多电极阵列,分布在很小的表面区域(~2*2 毫米)。mMPC的可伸缩性(高达500%)和柔韧性使其能够附着到hHO上。此外,我们还发现,在Wnt3a和SHH激活剂的诱导下,hHO产生了HOPX+和PAX6+祖先以及ZBTB20+PROX1+正中回颗粒神经元。hHO的转录组特征与发育中的人类海马体高度相似。我们成功地通过这种细胞类器官的mMPC检测到了hHO的神经活动。与传统的平面装置相比,我们的无创耦合技术为记录3D模型的神经信号提供了一种适配器。
创新点
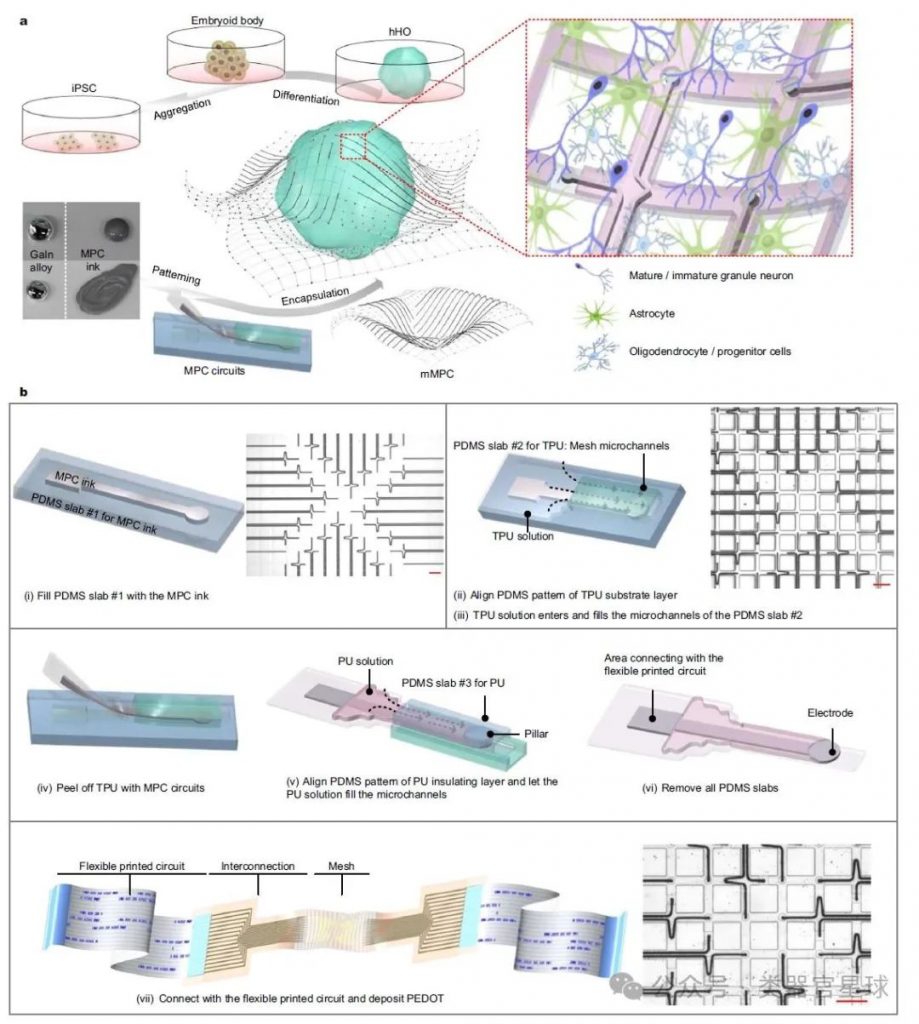
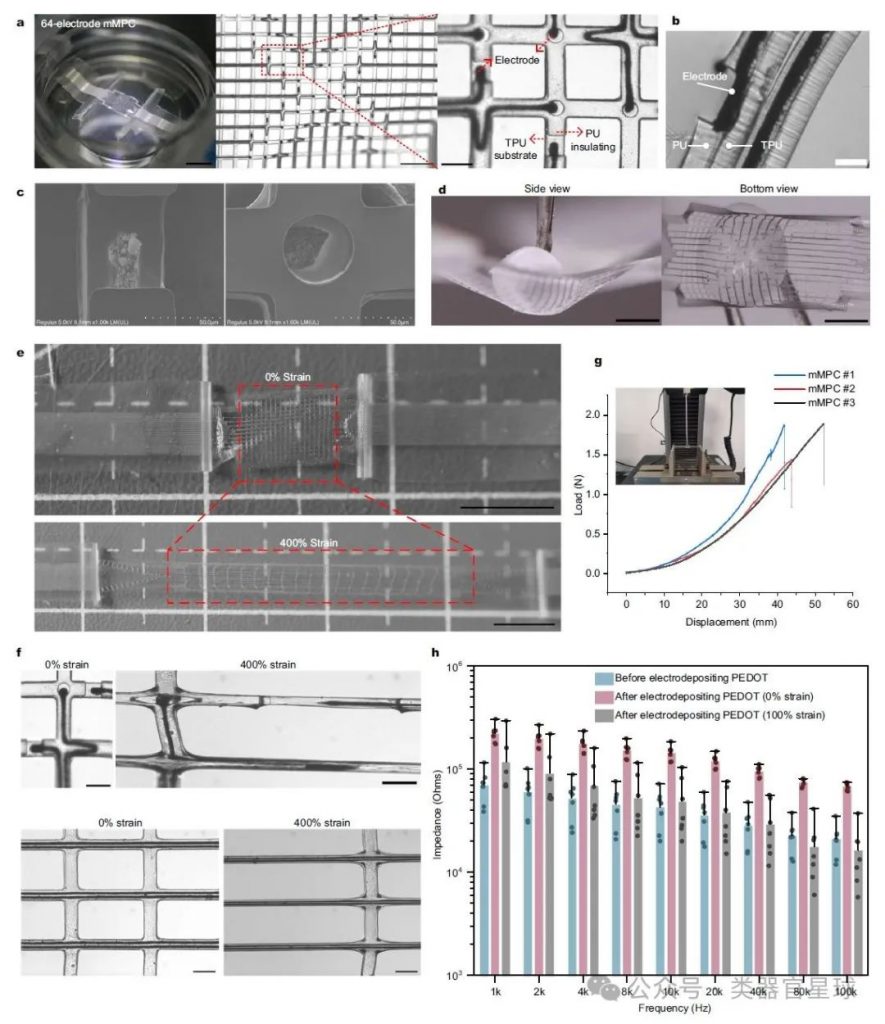
开发了一种基于液态金属-聚合物导体(MPC)的网格状神经界面(mMPC),该界面具有128通道的多电极阵列,分布在一个小的表面积(约2*2毫米)上。这种设计允许在非侵入性方式下获取hHO的电信号。
mMPC具有高达500%的可拉伸性,使其能够附着在hHO上,而不会影响其自然生长和形态。这种高伸缩性和灵活性是现有技术中不常见的。
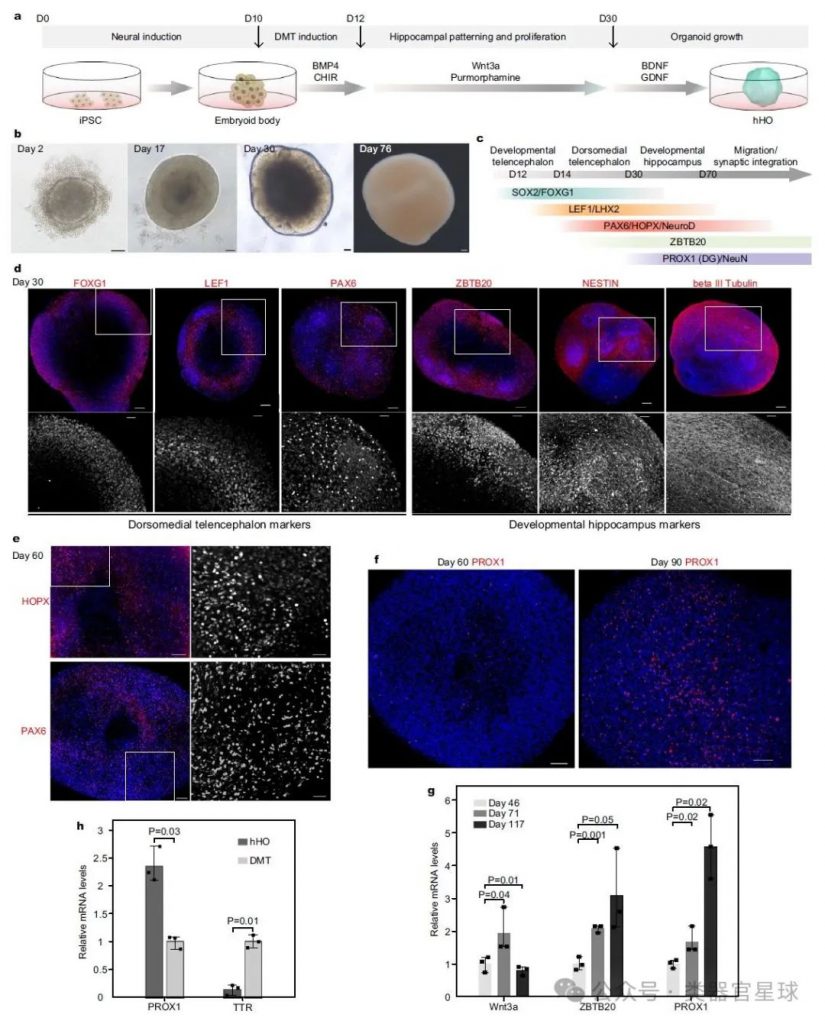
展示了在Wnt3a和SHH激活剂诱导下,hHO能够产生HOPX+和PAX6+前体细胞以及ZBTB20+PROX1+的齿状回颗粒神经元。这表明通过特定的信号通路诱导,可以更精确地控制hHO的发育和成熟。
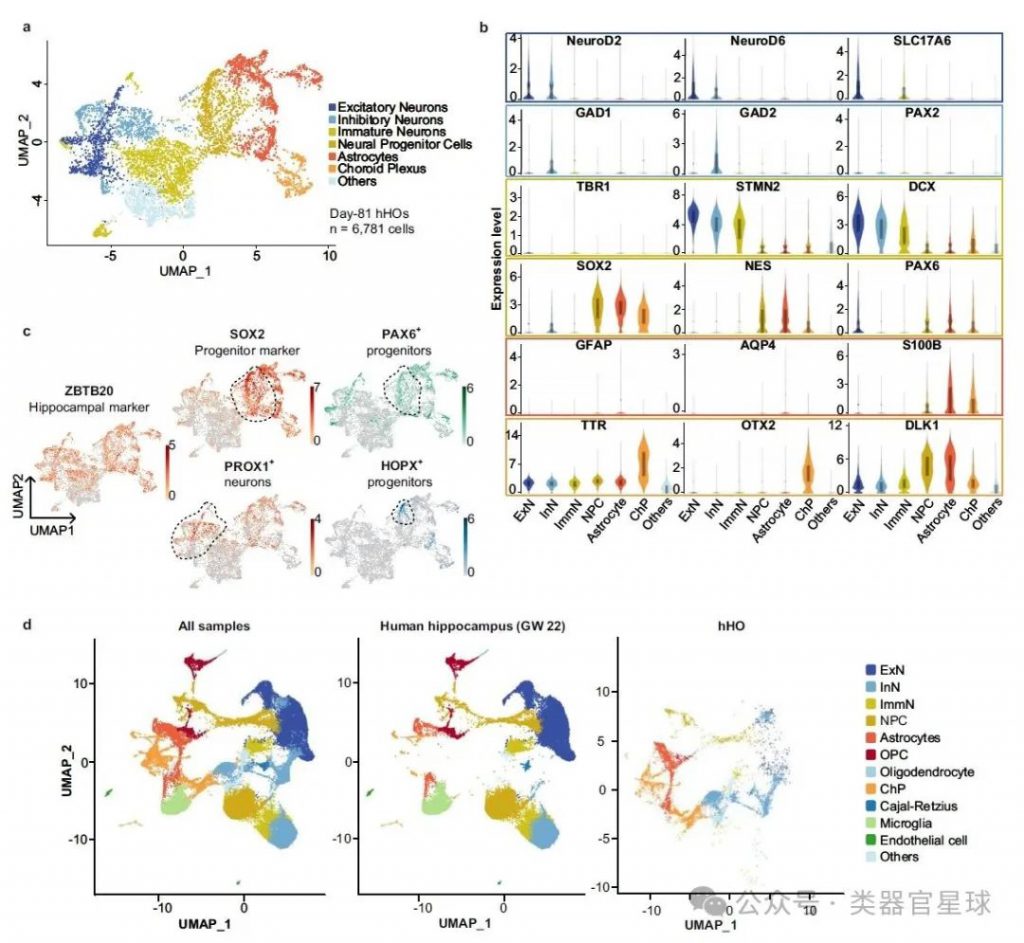
hHO的转录组特征与发育中的人类海马体高度相似,这为研究人类海马体的发育和疾病提供了重要的模型。
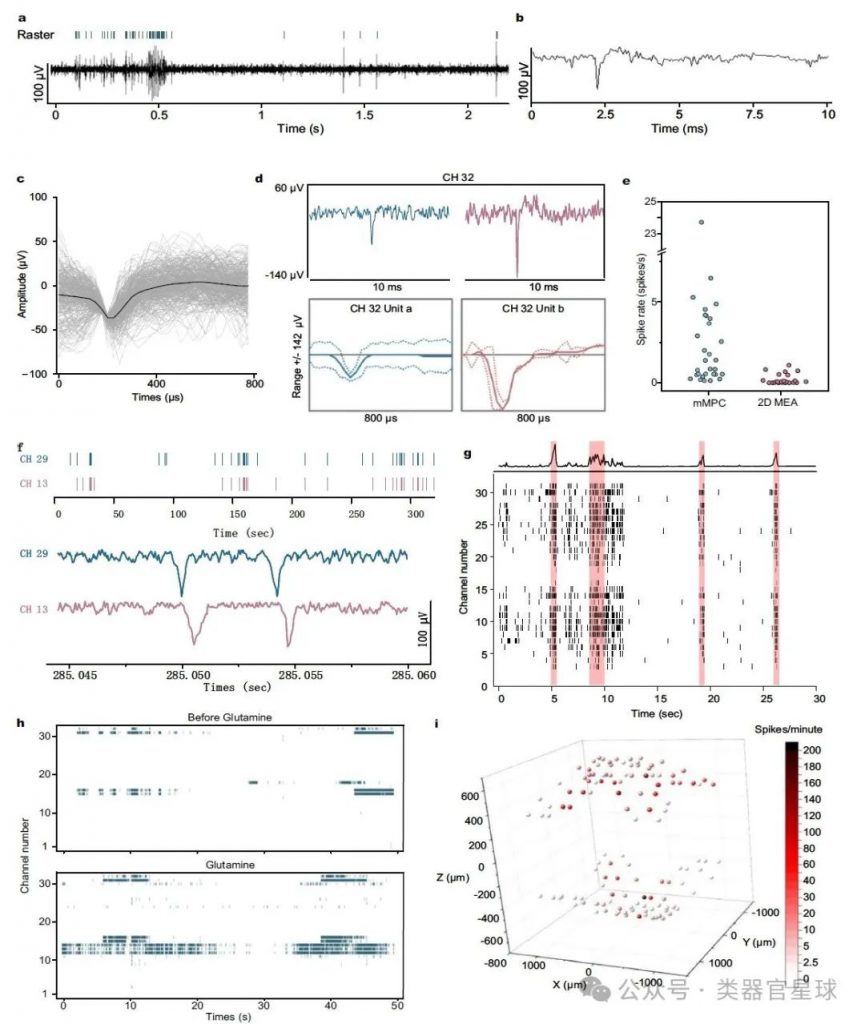
通过mMPC,研究者成功地从hHO中检测到神经活动,包括神经信号的同步和振荡网络活动。与传统的平面装置相比,这种非侵入性耦合提供了一种从3D模型中记录神经信号的适配器。
文献精读
Q1:这种新型的三维液态金属基神经界面(mMPC)如何实现与人类海马体类器官(hHO)的有效耦合?
A:mMPC通过其高度的伸缩性和灵活性能够紧密贴合在hHO的表面,同时保持对hHO自然生长和形态的影响最小。mMPC集成了128通道的多电极阵列,这些电极分布在一个小的表面积上,使得能够从hHOs中捕获更多的神经信号。此外,mMPC的网格状设计和液态金属-聚合物导体(MPC)的组成提供了必要的电导性,以实现有效的神经信号检测。
Q2:在研究中,如何通过改变信号通路诱导来提高hHO中特定神经元类型的产生?
A:研究中使用了Wnt3a和SHH激活剂来诱导hHO,这些信号通路在神经发育中起着关键作用。通过在特定时间点添加这些信号分子到培养基中,研究者能够促进hHO产生HOPX+和PAX6+前体细胞以及ZBTB20+PROX1+的齿状回颗粒神经元。这种方法允许更精确地控制hHO的区域特异性和细胞类型,从而模拟体内发育信号通路。
Q3:该研究如何证明hHO的转录组特征与发育中的人类海马体具有高度相似性?
A:研究者通过单细胞RNA测序(scRNA-seq)技术分析了hHO的转录组,并将结果与已发表的发育中人类海马体的数据集进行了比较。通过分析差异表达基因,研究者能够将细胞分群,并识别出与人类海马体发育过程中相似的细胞类型,包括兴奋性神经元、抑制性神经元、未成熟神经元、神经前体细胞、星形胶质细胞、少突胶质细胞前体和少突胶质细胞等。这种高度相似的转录组特征表明hHO能够模拟人类海马体的发育过程,为研究人类海马体提供了一个有力的模型系统
结果图





来第一个抢占沙发评论吧!